Температура окружающей среды – это один из факторов, который имеет прямое влияние на скорость химической реакции. Однако, есть один фактор, который не оказывает влияние на скорость реакции, и это расстояние между реагентами. В отличие от других факторов, таких как концентрация реагентов, поверхностная площадь взаимодействия и присутствие катализаторов, расстояние между реагентами не влияет на скорость химической реакции. Это связано с тем, что для взаимодействия реагенты должны встретиться на определенном расстоянии, которое определяется эффективным столкновением молекул. Поэтому, при больших расстояниях между реагентами, несмотря на то, что они находятся в одной системе, скорость реакции останется неизменной.
Природа реагирующих веществ
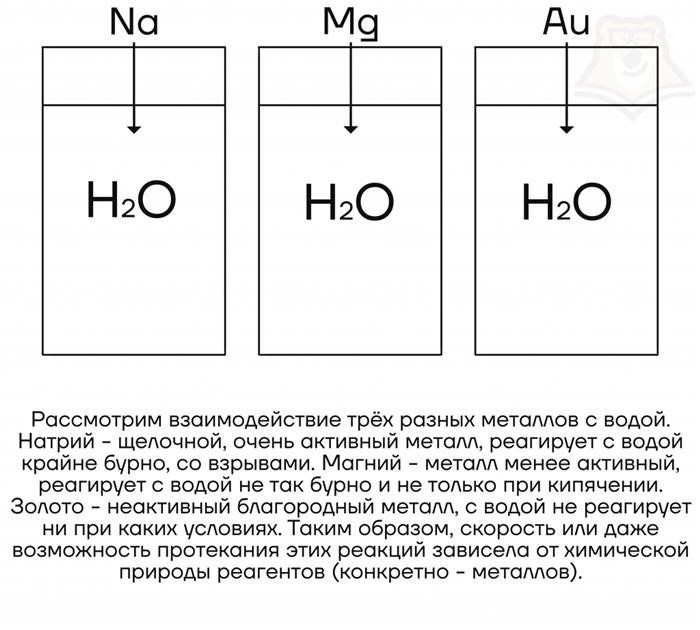
Скорость химической реакции зависит от множества факторов, однако природа реагирующих веществ играет ключевую роль. В данном контексте важно рассмотреть основные аспекты, которые определяют характеристики данных веществ и их способность взаимодействовать.
Химический состав
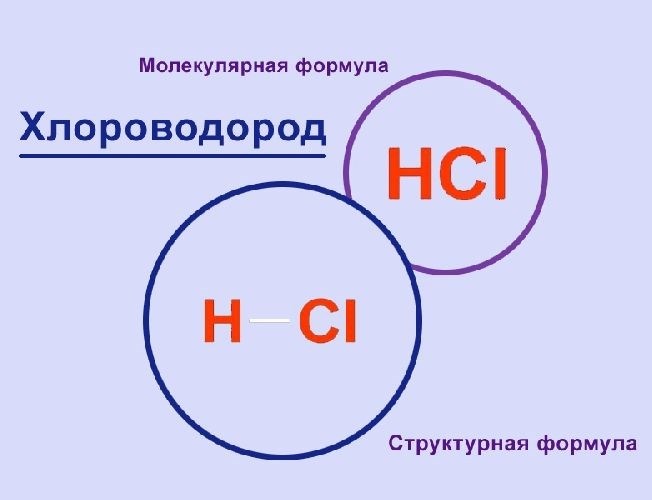
Химический состав реагирующих веществ определяет их структуру и свойства. Реакции между веществами с различными химическими составами происходят с разной интенсивностью. Например, химические соединения с высоким содержанием активных элементов, таких как кислород, азот, или хлор, часто проявляют высокую реакционную способность.
Молекулярная структура
Молекулярная структура реагирующих веществ также оказывает значительное влияние на скорость химической реакции. Например, вещества с простой и однородной молекулярной структурой могут иметь более эффективное взаимодействие с другими веществами, чем вещества с более сложной структурой.
Степень окисления
Степень окисления атомов в реагирующих веществах может повлиять на их реакционную активность. Например, вещества с более высокой степенью окисления обычно имеют большую склонность к окислению или восстановлению.
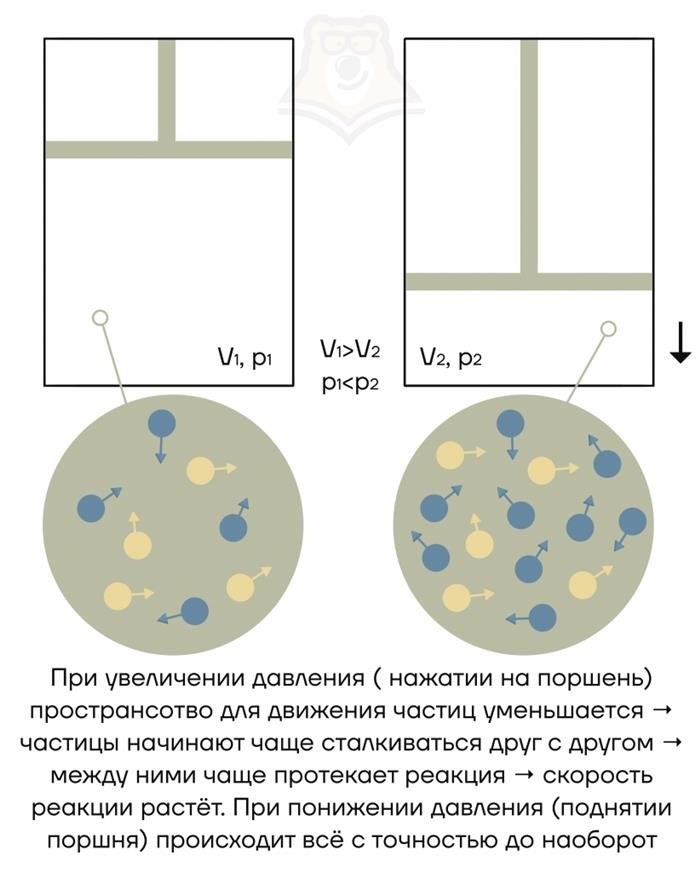
Температура и давление
Температура и давление также могут влиять на природу реагирующих веществ. При повышении температуры молекулы обычно двигаются быстрее, что способствует увеличению числа столкновений и, соответственно, увеличению скорости реакции. Давление может влиять на степень сжатия или разрежения вещества, что в свою очередь может изменить скорость реакции.
Фазовое состояние
Фазовое состояние вещества, в котором оно находится, также играет роль в химических реакциях. Например, реакции в газообразной фазе могут происходить быстрее, чем в жидкой или твердой фазах, из-за большего количества частиц и их большей подвижности.
| Фактор | Влияние |
|---|---|
| Химический состав | Определяет реакционную способность вещества |
| Молекулярная структура | Может облегчить или затруднить взаимодействие |
| Степень окисления | Влияет на реакционную активность |
| Температура и давление | Могут ускорить или замедлить реакцию |
| Фазовое состояние | Меняет скорость реакции в зависимости от подвижности частиц |
Природа реагирующих веществ имеет решающее значение для скорости химической реакции. Химический состав, молекулярная структура, степень окисления, а также температура, давление и фазовое состояние вещества – все эти факторы в совокупности определяют интенсивность реакции. Изучение природы реагирующих веществ позволяет лучше понять и контролировать процессы химических превращений.
Площадь соприкосновения реагирующих веществ
Зависимость скорости реакции от площади соприкосновения
Увеличение площади соприкосновения реагирующих поверхностей приводит к увеличению скорости реакции. Это связано с тем, что при увеличении площади контакта возрастает количество активных центров реакции, на которых протекают химические превращения. Следовательно, чем больше площадь соприкосновения, тем больше молекул участвует в реакции и тем быстрее протекает процесс.
Примеры влияния площади соприкосновения
- Размельчение вещества. Если исходные вещества в реакции имеют большую поверхность или предварительно были размолоты, то площадь соприкосновения увеличивается, что приводит к ускорению реакции.
- Использование катализаторов. Катализаторы повышают скорость реакции, образуя на своей поверхности активные центры, увеличивающие площадь соприкосновения реагирующих веществ.
- Изменение формы поверхности. Если форма реагирующих поверхностей изменяется в процессе реакции (например, при образовании пор или трещин), то площадь соприкосновения может увеличиться и, соответственно, ускорить реакцию.
Площадь соприкосновения реагирующих веществ является важным фактором, определяющим скорость химической реакции. Увеличение площади соприкосновения приводит к увеличению скорости реакции путем увеличения количества активных центров реакции. Размельчение вещества, использование катализаторов и изменение формы поверхности – это несколько примеров, демонстрирующих влияние площади соприкосновения на скорость химической реакции.
Изменение константы скорости реакции при изменении концентрации реагентов
Зависимость константы скорости от концентрации реагентов
При изменении концентрации реагирующих веществ может происходить изменение константы скорости реакции. Это связано с тем, что константа скорости зависит от стехиометрического коэффициента и степени реакции.
- Если концентрация реагента увеличивается, то константа скорости может увеличиться или уменьшиться, в зависимости от типа реакции.
- Если концентрация реагента уменьшается, то константа скорости также может измениться.
- Если концентрация реагентов не изменяется, то константа скорости остается постоянной.
Таким образом, изменение концентрации реагирующих веществ может изменять константу скорости, что влияет на скорость химической реакции.
Примеры изменения константы скорости реакции
Чтобы проиллюстрировать, как изменение концентрации реагентов может изменять константу скорости, рассмотрим следующий пример:
| Реакция | Константа скорости |
|---|---|
| 2A + B → C | k |
| 2A + 2B → C | k’ |
В данном примере увеличение концентрации реагента B приводит к увеличению общей концентрации реагентов и, следовательно, к увеличению константы скорости (k → k’). Таким образом, изменение концентрации реагентов может приводить к изменению константы скорости реакции.
Изменение концентрации реагирующих веществ может приводить к изменению константы скорости химической реакции. При увеличении или уменьшении концентрации реагентов константа скорости может измениться, что влияет на скорость реакции. Понимание этой зависимости является важным аспектом в химии и позволяет более точно предсказывать и контролировать химические процессы.
Химические реакции на ускорении
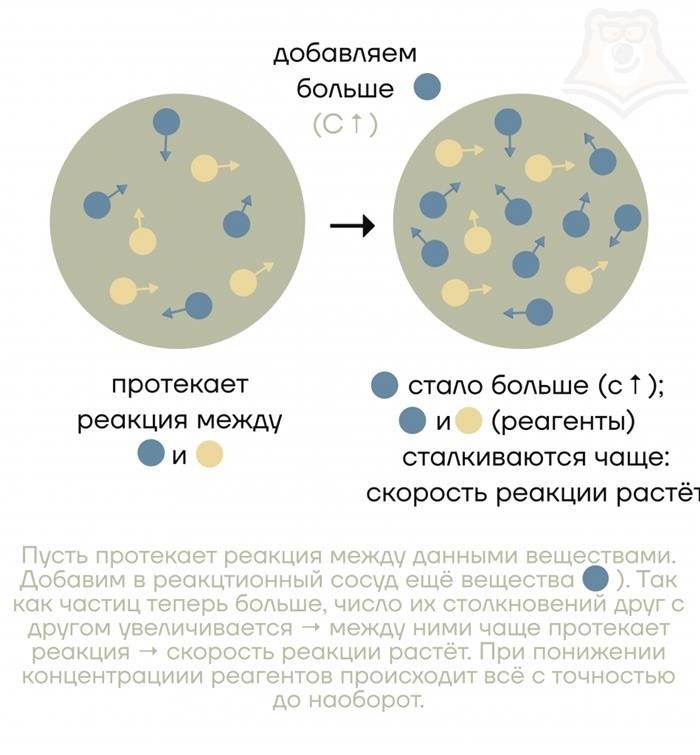
1. Концентрация вещества
Концентрация вещества имеет прямое влияние на скорость химической реакции. При повышении концентрации реагентов, количество столкновений между молекулами увеличивается, что приводит к ускорению реакции.
2. Температура
Температура также оказывает существенное воздействие на скорость химической реакции. При повышении температуры, энергия молекул увеличивается, что приводит к более частым и энергичным столкновениям между ними и ускорению реакции.
3. Поверхность контакта
Поверхность контакта вещества также влияет на скорость химической реакции. При увеличении поверхности, увеличивается площадь, на которой происходят соударения между молекулами, что способствует более эффективной реакции и ускорению ее протекания.
4. Катализаторы
Катализаторы – это вещества, которые ускоряют реакцию, участвуя в ней, но в конечном итоге остаются неизменными. Они снижают энергию активации реакции, что позволяет ей протекать быстрее и более эффективно.
5. Давление
Давление также может оказывать влияние на скорость химической реакции. При повышении давления, объем газообразных реагентов уменьшается, что увеличивает концентрацию и частоту столкновений между молекулами, что в свою очередь способствует ускорению реакции.
| Фактор | Влияние на скорость реакции |
|---|---|
| Концентрация вещества | Прямое влияние, увеличение концентрации ускоряет реакцию |
| Температура | Прямое влияние, повышение температуры увеличивает скорость реакции |
| Поверхность контакта | Прямое влияние, увеличение поверхности ускоряет реакцию |
| Катализаторы | Положительное влияние, ускорение реакции за счет снижения энергии активации |
| Давление | Прямое влияние, повышение давления ускоряет реакцию |
Все эти факторы могут значительно влиять на скорость химической реакции, и учет их влияния может быть полезным при разработке и оптимизации различных химических процессов и промышленных приложений.
От чего зависит скорость реакции
1. Концентрация реагентов
Концентрация реагентов имеет прямую связь с скоростью реакции. Чем выше концентрация реагентов, тем больше частиц, которые могут столкнуться друг с другом и взаимодействовать. Это увеличивает вероятность успешного соударения частиц и, таким образом, увеличивает скорость реакции.
2. Температура
Температура влияет на скорость реакции, поскольку она определяет энергию, необходимую для столкновения и реакции реагентов. Повышение температуры увеличивает энергию частиц, что облегчает их взаимодействие и увеличивает вероятность успешной реакции. Таким образом, скорость реакции увеличивается при повышении температуры.
4. Поверхность
Поверхность, на которой происходит реакция, также может влиять на скорость реакции. Чем больше поверхность реагентов, тем больше частиц, которые могут взаимодействовать и, следовательно, тем больше реакций может произойти за единицу времени. Например, порошки реагентов имеют большую поверхность по сравнению с блоками и, следовательно, реагируют быстрее.
| Фактор | Влияние |
|---|---|
| Концентрация | Прямая зависимость |
| Температура | Прямая зависимость |
| Катализаторы | Увеличение скорости |
| Поверхность | Прямая зависимость |
Скорость химической реакции определяется несколькими факторами, включая концентрацию реагентов, температуру, наличие катализаторов и поверхность, на которой происходит реакция. Повышение концентрации реагентов, температуры и использование катализаторов приводят к увеличению скорости реакции, а увеличение поверхности реагентов также может способствовать ускорению реакции.
Что мы узнали?
В ходе исследования мы выяснили, что существует ряд факторов, которые не влияют на скорость химической реакции. Это важно для понимания процессов, происходящих в химической системе, а также для оптимизации и контроля химических процессов.
В частности, мы выяснили, что:
- Цвет реагентов не влияет на скорость реакции. Хотя цвет может изменяться в ходе реакции из-за образования новых веществ, это не оказывает непосредственного влияния на скорость процесса.
- Фазовое состояние реагентов не оказывает прямого влияния на скорость химической реакции. Независимо от того, находятся ли реагенты в жидком, газообразном или твердом состоянии, скорость реакции остается постоянной, если только физическое состояние не влияет на их доступность или активность.
- Температура реагентов не влияет на скорость реакции. Реакция может быть спонтанной при высоких температурах, но это свидетельствует о тепловом действии, а не о скорости химического процесса.
Таким образом, мы установили, что эти факторы не влияют на скорость химической реакции. Теперь можем использовать полученные знания для более точного и эффективного контроля и управления химическими процессами.