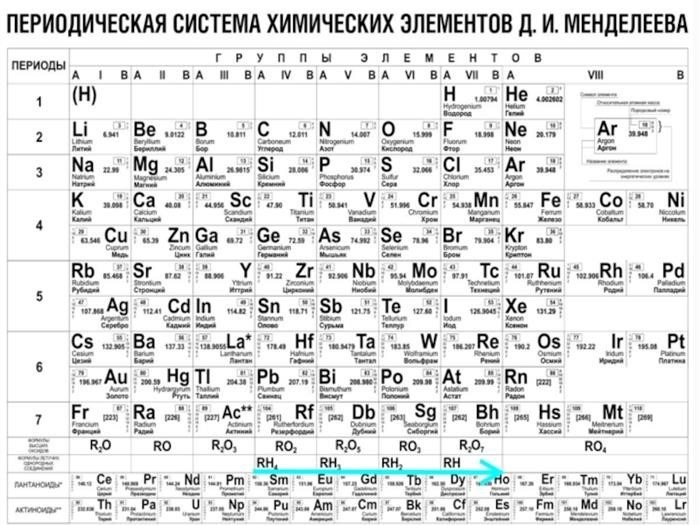
Периодическая таблица Менделеева – это важный инструмент для химиков и физиков, который позволяет организовать и систематизировать знания об элементах и их свойствах. Однако существует несколько других форм периодической таблицы Менделеева, которые предлагают альтернативные способы организации элементов. В данной статье будут представлены эти формы и проведена презентация, открывающая новые возможности и перспективы для научного исследования и обучения.
Объяснительная и предсказательная функции Периодического закона
Объяснительная функция Периодического закона
Периодический закон объясняет регулярные закономерности в свойствах элементов и помогает понять их атомную структуру и взаимодействия. Согласно этому закону, элементы расположены в порядке возрастания атомных номеров в периодической таблице, а их свойства меняются циклически.
- Размещение элементов в периодической таблице: Периодический закон объясняет способ размещения элементов в таблице. Он показывает, что элементы разделены на периоды (горизонтальные ряды) и группы (вертикальные столбцы) в зависимости от их общих электронных конфигураций.
- Зависимость свойств элементов: Периодический закон объясняет, почему элементы в определенных группах имеют сходные свойства. Например, элементы группы щелочных металлов имеют одинаковую валентность и образуют сильные щелочи. Это объясняется наличием одного электрона во внешней оболочке.
- Поиск новых элементов: Периодический закон помогает предсказать свойства и возможную существование еще неизвестных элементов. Например, Дмитрий Менделеев использовал этот закон для предсказания свойств и характеристик неизвестных на тот момент элементов, какими впоследствии они оказались на самом деле.
Предсказательная функция Периодического закона
Периодический закон имеет предсказательную функцию, позволяющую определить свойства и реакционную способность элементов в периодической таблице на основе их положения.
| Период | Щелочные металлы | Щелочноземельные металлы | Переходные металлы |
|---|---|---|---|
| 1 | Литий (Li) | Бериллий (Be) | – |
| 2 | Натрий (Na) | Магний (Mg) | – |
| … | … | … | … |
- Свойства элементов: Периодический закон позволяет предсказывать подобные свойства элементов в пределах одной группы. Например, все щелочные металлы имеют низкую плотность, низкую температуру плавления и высокую реакционную способность.
- Валентность элементов: Периодический закон предсказывает валентность элементов и их возможность образовывать химические соединения. Например, элементы из группы щелочных металлов всегда имеют валентность +1, а элементы из группы галогенов имеют валентность -1.
- Восстановительная и окислительная способности: Периодический закон предсказывает относительную восстановительную и окислительную способность элементов. Например, щелочные металлы имеют сильную восстановительную способность, а неметаллы из группы галогенов – сильную окислительную способность.
Объяснительная и предсказательная функции Периодического закона играют важную роль в полном понимании и исследовании свойств элементов и их химических реакций. Этот закон стал фундаментом для развития химии и образования периодической таблицы Менделеева, которая до сих пор служит основным инструментом для организации и изучения химических элементов.
Структура периодической таблицы Менделеева
Периодическая таблица Менделеева представляет собой удобное упорядоченное представление химических элементов. Она состоит из строк, называемых периодами, и столбцов, называемых группами. Таблица имеет свою структуру, основанную на свойствах элементов и их атомной структуре.
Периоды таблицы
Периоды таблицы представляют собой горизонтальные строки, которые разделяют элементы на основе количества электронных оболочек. Каждый новый период начинается с заполнения очередной электронной оболочки. Всего в таблице существуют 7 периодов.
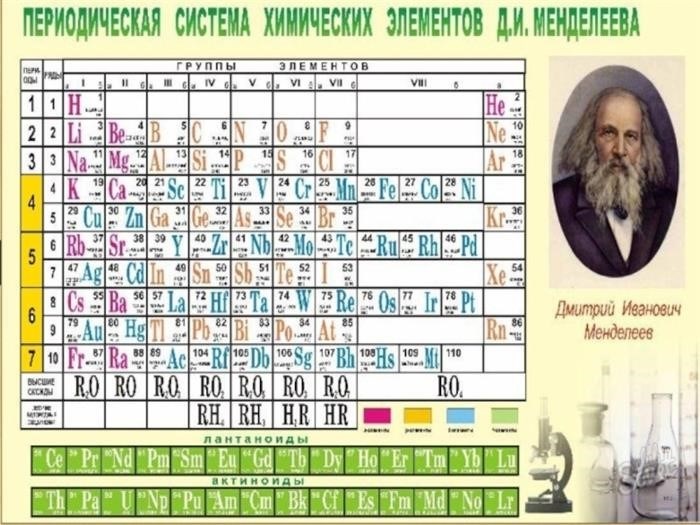
Группы таблицы
Группы таблицы представляют собой вертикальные столбцы, которые разделяют элементы на основе их электронной конфигурации и химических свойств. Группы обозначаются числами и буквами, например, группа 1A или 2B. В таблице существует 18 групп.
Наиболее распространенные формы таблицы
Периодическая таблица Менделеева существует в различных формах, которые используются для разных целей и в разных областях науки:
- Классическая форма – самая распространенная и знакомая форма таблицы, где элементы расположены в порядке возрастания атомного номера. Она несет в себе информацию о химических символах элементов, атомных массах и периодическом законе.
- Круговая форма – таблица представлена в виде круга, где группы элементов образуют окружности, а периоды расположены по радиусам. Это удобная форма для визуального представления связей между элементами.
- Таблица Менделеева-Риддела – модификация классической формы таблицы, где элементы расположены в порядке возрастания атомных номеров, а также по сходству химических свойств и химической активности.
Цитата о периодической таблице Менделеева
“Периодическая таблица Менделеева – великое достижение науки, которое помогает нам понять и классифицировать многообразие химических элементов. Ее структура и формы представления позволяют легко найти нужную информацию и проводить исследования в разных областях химии и физики.”

Количество элементов, ряды
Элементы периодической таблицы Менделеева разделены на 7 горизонтальных строк, которые называются рядами. Первый ряд состоит из 2 элементов – водорода (H) и гелия (He). Второй ряд состоит из 8 элементов, третий – из 8 элементов и так далее. Седьмой ряд, самый длинный, содержит 32 элемента.
По мере увеличения номера ряда, элементы становятся все более сложными и тяжелыми. В каждом ряду элементы имеют схожие химические свойства и поэтому могут быть классифицированы как одна группа.
Итак, периодическая таблица Менделеева представляет собой огромное разнообразие элементов, структурированных на основе их атомных свойств. Она является основой для понимания и изучения химических процессов и свойств материи.